Metalik Bağ 9. Sınıf Kimya
METALİK BAĞ
Metal atomlarının en dış kabuğunda az sayıda elektron vardır. İç elektronlar çekirdeğin artı yükünün etkisini azaltırlar ve bir bakıma en dış elektronlar, çekirdeğin çekme kuvvetine karşı korunur. Bu nedenle en dış elektronlar çekirdek tarafından kuvvetle çekilmezler.
Bir metal kristalindeki atomlar çekirdek ve iç elektronların meydana getirdiği kararlı bir kısım ile bu kısım tarafından zayıf bir kuvvetle çekilen en dış elektronlardan (valans elektronu) yapılmış olarak düşünülebilir. Örneğin sodyum atomunda 11 elektron vardır ve bu elektronlardan on tanesi iç elektrondur. Çekirdekte 11 proton olduğuna göre sodyum atomunun artı bir yüklü bir kısım (çekirdek ve 10 elektron) ile bir dış elektronun meydana geldiğini söyleyebiliriz.
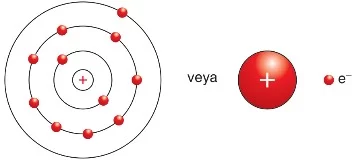
Katı hâldeki bir metale atomlar birbirlerine çok yakın olacaklarından en dış elektronlar diğer atomların etki alanına girerler. Artık bu elektronları belirli atomların elektronları değil de diğer atomların etrafında serbest halde bulunan elektronlar şeklinde düşünmek doğru olur. O halde atomları iç kısmının oluşturduğu artı yüklü kürecikler, dış elektronların meydana getirdiği bir elektron bulutunun içinde dizilmişlerdir.
Metallerin değerlik elektronları serbest hareket edebilir ve hem kendi çekirdekleri hem de diğer atomların çekirdekleri etrafında dolanırlar. Metal atomlarında oluşan bu durumu bir elektron denizi oluştuğu şeklinde düşünebiliriz.
Bir metal atomu değerlik elektronlarını elektron denizine vermiş ve (+) yüklü katyon hâline gelmiştir.
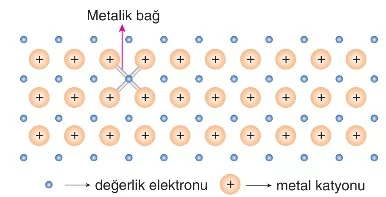
Oluşan metal katyonu ile elektron denizindeki hareketli elektronlar arasındaki çekim kuvvetine metalik bağ denir.
Metalik bağın metallere kazandırdığı özellikler
- Hareketli elektronların sayesinde ısı ve elektrik akımını iyi iletirler. Metallerin elektrik akımını iletmesi şu şekilde açıklanabilir:
Metaldeki elektronlar serbesttir ve hareketlidirler. Bu yüzden, bir metalin ucundan, bir dış kaynaktan, elektron girdiğinde serbest hâldeki hareketli elektronlar telin içinden geçerek telin diğer ucundan aynı şekilde çıkarlar. - Hareketli elektronların ışığı yansıtmasından dolayı yüzeyleri parlaktır.
- Hareketli elektronlar sayesinde tel ve levha hâline getirilebilirler.
- Serttirler. Metalik bağın kuvveti arttıkça, metalin sertliği de artar.
- Esnektirler, dövülebilir ve şekillendirilebilirler.
Metallerin dövülüp şekillendirilebilmesi şu şekilde açıklanabilir:
Metal iyonlarının bir tabakası darbe ile diğerine karşı kaymaya gelmeye zorlanırsa hiçbir bağı kırılmaz, metalin iç yapısı, esas olarak, değişmeden kalır ve elektron denizi hızla yeni duruma uyum sağlar.
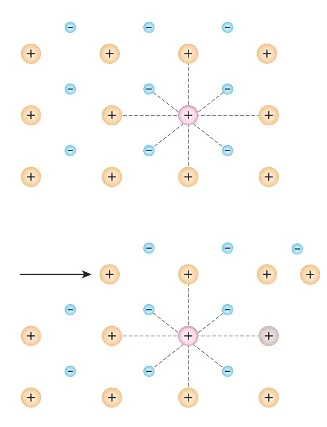
Görsel açıklaması: Görsele göre bir metale kuvvet uygulandığında (soldan sağa doğru), katyonların yeri değişir ama yakın çevresi değişmez. Elektron denizi modeli metallerin şekil değiştirme kolaylıklarını açıklar.
- Metal atomları metalik bağ ile bir araya gelerek kristal yapı oluşturur.
- Metalik bağ saf metallerde bulunabileceği gibi metallerin oluşturduğu homojen karışımlar olan alaşımlarda da (örneğin; tunç, lehim) bulunur.
Metalik bağ gücü nelere bağlıdır?
Aynı koşullarda sodyum metalinin erime noktası 98°C iken, magnezyum metalinin erime noktası 649°C’dir. Bunun temel olarak üç nedeni vardır.
Birincisi magnezyum “2+” iyonu oluştururken, sodyum “1+” iyonu oluşturur. Bu sayede magnezyum metalinde değerlik elektronları ve katyonlar arasında daha güçlü bir elektrostatik çekim gücü oluşmuştur.
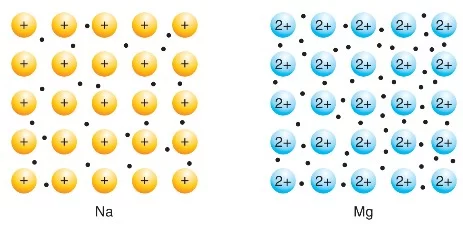
İkinci nedeni de Mg²⁺ iyon yarıçapı 65 pm iken, Na⁺ iyon yarıçapı 98 pm’dir. Yarıçap azaldıkça değerlik elektronları pozitif iyonun çekirdeğine daha çok yaklaşır ve daha güçlü çekilir.
Nedenlerden üçüncüsü de magnezyumda atom başına 2 serbest elektron bulunurken, sodyumda bu sayı 1’dir. Bu sayede Mg metalinde iyonlar ve serbest elektronlar arasındaki elektrostatik çekim gücü daha fazladır denilebilir.
Sonuç olarak:
Metalik bağ gücü nelere bağlıdır?
Metalik bağ kuvveti,
- Değerlik elektron sayısı arttıkça artar.
- Atom yarıçapı azaldıkça artar.
Metalik bağ gücü ile metalin erime noktası doğru orantılıdır. Metallerin bağ gücü artarsa, metallerin erime noktası artar.
Periyodik cetvelde; belirtilen ok yönlerinde metalik bağ gücü artar.
9. Sınıf Metalik Bağ Konu anlatımı özet örnekler Ders Notları
Metaller, günlük yaşamımızın vazgeçilmez bir parçasıdır. Elektronik cihazlardan inşaat malzemelerine kadar birçok alanda kullanılırlar. Metallerin bu kadar yaygın ve dayanıklı olmasının sebebi, atomları arasında oluşan metalik bağlardır. Metalik bağ, metal atomları arasında oluşan özel bir kimyasal bağ türüdür. Bu makalede, metalik bağın ne olduğunu, nasıl oluştuğunu ve metallerin özelliklerine nasıl katkıda bulunduğunu inceleyeceğiz.
Metalik Bağın Tanımı
Metalik bağ, metal atomları arasında serbestçe hareket edebilen ve atomlar arasında paylaşılan elektronlar sayesinde oluşan bir bağ türüdür. Metallerde, atomların dış enerji seviyesindeki elektronlar, atomlar arasında serbestçe hareket edebilirler. Bu serbest hareket eden elektronlar "elektron denizi" olarak adlandırılır ve metalik bağı oluşturur. Bu elektron denizi, metal atomlarını bir arada tutar ve metalin yapısal bütünlüğünü sağlar.
Metalik Bağın Oluşumu
Metallerin atomları, kristal yapılar oluşturacak şekilde sıkı bir şekilde paketlenir. Her metal atomu, komşu atomlarıyla elektronlarını paylaşır ve bu elektronlar metalin tüm yapısında serbestçe hareket edebilir. Bu sayede, metal atomları arasında güçlü bir çekim kuvveti oluşur. Metalik bağın gücü, metalin erime noktası, sertliği ve elektriksel iletkenliği gibi özelliklerini belirler.
Metalik Bağın Özellikleri
- Elektriksel İletkenlik: Metalik bağ sayesinde metaller iyi birer elektrik iletkenidir. Elektron denizindeki serbest elektronlar, elektrik akımını iletmek için metal boyunca kolayca hareket edebilir.
- Isıl İletkenlik: Metallerin ısıl iletkenliği de yüksek düzeydedir. Serbest elektronlar, ısının metal boyunca hızla yayılmasını sağlar.
- Parlaklık: Metal atomları arasında serbestçe hareket eden elektronlar, metallere parlak ve yansıtıcı bir yüzey kazandırır. Bu özellik, metallerin ışığı iyi yansıtabilme yeteneğinden kaynaklanır.
- Dövülebilirlik ve Çekilebilirlik: Metalik bağın esnek yapısı, metallerin dövülebilir ve çekilebilir olmasını sağlar. Metaller, kolayca şekil alabilir ve ince tel veya levha haline getirilebilir.
- Yüksek Erime ve Kaynama Noktaları: Metalik bağın gücü, metallerin yüksek erime ve kaynama noktalarına sahip olmasına neden olur. Bu özellik, metal atomları arasındaki güçlü çekim kuvvetlerinden kaynaklanır.
Metalik Bağın Önemi
Metalik bağ, günlük hayatta kullandığımız birçok metalin özelliklerini belirler. Örneğin:
- Elektrik kabloları: Bakır gibi iyi iletken metaller, elektrik enerjisini taşımak için kullanılır.
- Yapı malzemeleri: Çelik gibi metaller, binaların ve köprülerin inşasında kullanılır.
- Mutfak eşyaları: Paslanmaz çelik gibi metaller, dayanıklı ve hijyenik olduğu için mutfak eşyalarında kullanılır.
Metalik bağ, metallerin dayanıklı, esnek ve iletken olmasını sağlayan temel bir kimyasal bağ türüdür. Bu bağ, serbestçe hareket eden elektronlar sayesinde metal atomlarını bir arada tutar ve metallere karakteristik özelliklerini kazandırır. Metalik bağın bu özelliklerini anlamak, metallerin günlük hayatta neden bu kadar yaygın kullanıldığını ve hangi özelliklere sahip olduklarını açıklamaya yardımcı olur.