Periyodik Tabloda Yer Bulma 9. Sınıf Kimya
- Periyodik tabloda yatay sıralara periyot, dikey sütunlara ise grup adı verilir. Periyodik tabloda 7 periyot ve 18 grup bulunur. Bu 18 grubun 8’i A grubu, 10’u ise B grubudur.
- Aynı grupta bulunan elementler, genellikle benzer kimyasal özelliklere sahiptir.
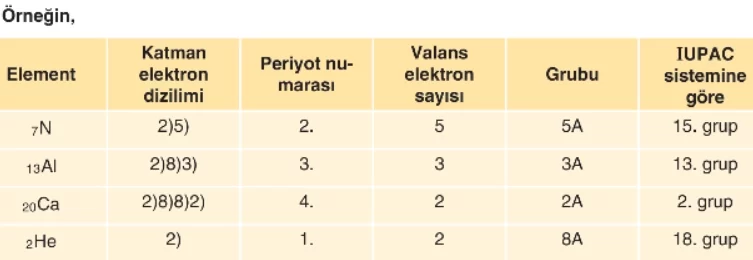
- Bir elementin periyodik sistemdeki periyot numarası, en büyük enerji düzeyini (katman numarasını) gösterir. Grup numarası ise elementin değerlik (valans) elektron sayısıdır. Örneğin, ‘nin değerlik elektron sayısı 2’dir ve periyodik tabloda 8A grubunda yer alır.
- IUPAC sistemine göre, periyodik tabloda gruplar 1’den 18’e kadar numaralandırılır; bu gruplar 1. grup, 2. grup, … , 18. grup şeklinde adlandırılır.
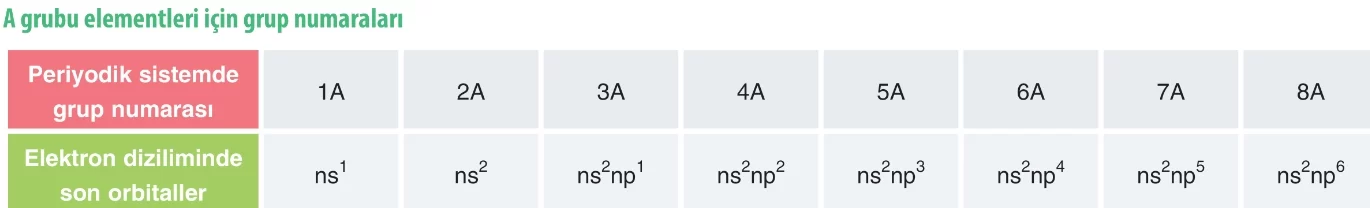
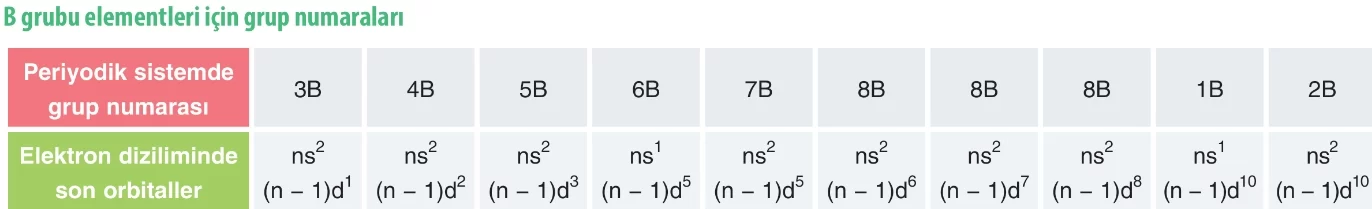
Bir elementin periyodik cetveldeki yeri belirlenirken temel hâl elektron dizilimi kullanılır.
- Enerji katman numarası
ise bir katmanda bulunabilecek en fazla elektron sayısı
formülü ile bulunur. Buna göre:
- Enerji katmanında (n = 1) en fazla
tane elektron bulunur.
- Enerji katmanında (n = 2) en fazla
tane elektron bulunur.
- Enerji katmanında (n = 3) en fazla
tane elektron bulunur.
- Enerji katmanında (n = 4) en fazla
tane elektron bulunur.
- Enerji katmanında (n = 1) en fazla
Atom numarası 20’ye kadar olan atomların katman elektron dizilimleri yapılırken şu kurallara uyulur:
- İlk 2 elektron 1. katmana yerleştirilir.
- i. İçten dışa doğru enerji seviyeleri doldurulurken her seferinde geriye kalan elektron sayısı hesaplanır.
- ii. Elde kalan elektron sayısı 8 veya daha az ise tamamı 2. katmana yerleştirilir.
Örnek: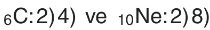 iii. Elde kalan elektron sayısı 16’dan az ise 2. katmana 8 elektron, 3. katmana ise kalan elektronlar yerleştirilir.
iii. Elde kalan elektron sayısı 16’dan az ise 2. katmana 8 elektron, 3. katmana ise kalan elektronlar yerleştirilir.
Örnek: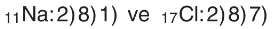
iv. Elde kalan elektron sayısı 17 ya da 18 ise 2. ve 3. katmana 8’er elektron yazılırken 4. katmana kalan elektronlar yerleştirilir.
Örnek: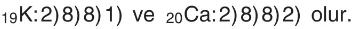
Buna göre atom numarası 20’ye kadar olan atomların temel hâl katman elektron dizilimi bu tabloya göre yapılır.
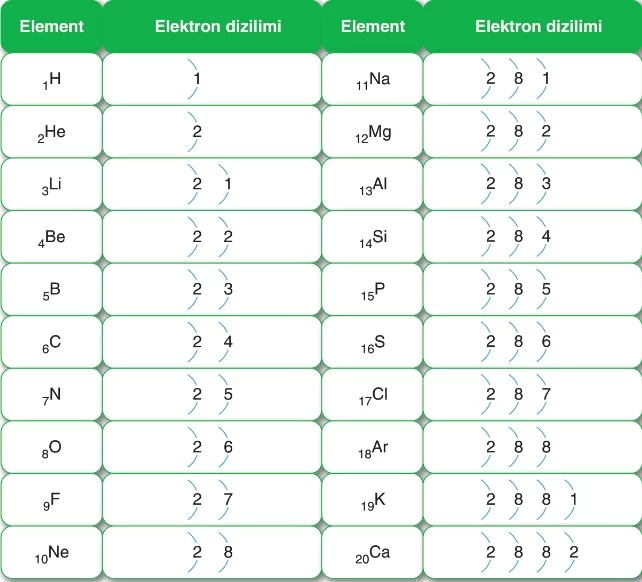
- Elementlerin temel hâl katman elektron dizilimindeki en son katmandaki toplam elektron sayısına Valans (değerlik) elektron sayısı denir.
Örneğin,4) için valans elektron sayısı 4 iken,
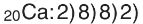 için bu değer 2’dir.
için bu değer 2’dir.
atomunun valans elektron sayısı 2’dir.
- Atomlar bağ oluştururken valans elektronlarını kullanırlar.
- Valans elektron sayısı, atomun kimyasal özelliklerinin belirlenmesinde önemli bir rol oynar.
- Elementlerin temel hâl elektron dizilimindeki katman sayısı, elementin periyodunu, valans elektron sayısı ise grubunu verir.
BİR YORUM YAZIN
ZİYARETÇİ YORUMLARI - 0 YORUM